药品安全“隐形守门人”|毒理学评估:从源头到终端,守护每一粒药的安全底
浏览量:16次
药品安全无小事,每一片能放心抵达患者手中的药,都藏着一道不为人知的“安全关卡”——毒理学评估。它不是临床试验的光环焦点,却是贯穿药品研发、生产、上市全生命周期的核心风控屏障。作为天鉴检测毒理学专家,我们常年以科学数据为盾,为药品质量安全筑牢第一道防线。
今天,我们用权威定义+经典案例,带你看懂:毒理学评估如何为药品安全“排雷”、“控险”、“护航”。

什么是药品毒理学评估?
药品毒理学评估,是通过体外试验、动物实验、安全评估等标准化科学手段,系统研究药品原料、辅料、工艺杂质、降解产物、残留溶剂等对生物体的毒性效应,精准明确:
是否有毒、毒性类型与作用强度;
毒性靶器官与作用机制;
安全剂量范围与风险阈值;
特殊人群(孕妇、儿童、老人)用药风险。
正如“毒理学之父”帕拉塞尔苏斯所言:“一切物质都是毒物,无毒与有毒仅在于剂量。”毒理学评估的核心并非“一票否决”,而是科学界定安全边界、实现风险可控,这也是它与普通“毒物检测”最本质的区别——最终让药品实现“疗效—风险比”最优。

图1 非临床哺乳动物毒性试验
贯穿药品全生命周期,每一步都不可或缺
毒理学评估不是“一次性检测”,而是贯穿药品研发、生产、上市后监管的“全程护航”,不同阶段的评估重点不同,但核心目标一致——守住药品质量安全底线。结合经典案例,我们逐一拆解关键应用场景。
应用一:研发初期排雷,避免无效投入与安全隐患
药品研发的第一步,就是通过毒理学评估筛选候选化合物:淘汰毒性过大、安全窗口过窄的成分,保留“疗效明确、毒性可控”的候选药。这一步不仅能避免后续研发的无效投入,更能从源头规避潜在的安全风险。
这里必须提到一个里程碑式的反面案例——沙利度胺(反应停)事件,它直接推动了现代药品毒理学评估体系的建立。

图2 反应停“海豹肢”婴儿
上世纪50年代,德国格兰泰制药研发的沙利度胺,因镇静、止吐效果显著,被当作“安全无毒”的非处方药上市,广泛用于缓解孕妇早孕反应,广告语甚至声称“孕妇及儿童均可服用,实验室中未能找到小鼠的致死剂量”。但当时,企业仅做了简单的急性毒性试验,未开展生殖毒性评估,也未关注不同物种对药物的毒性差异——沙利度胺对小鼠致畸性较弱,但对人类等灵长类动物却有极强的致畸性。
最终,这一“未完成毒理学评估”的药品,导致全球超过1万名新生儿出现“海豹肢畸形”(肢体发育不全,像海豹鳍一样),流产、早产、死胎不计其数,成为世界药物史上最惨痛的药害事件之一。
沙利度胺事件的惨痛教训,让全球意识到:药品研发初期的毒理学评估(尤其是生殖毒性、特殊毒性评估)不可或缺。如今,所有候选药物在进入临床试验前,必须完成急性毒性、长期毒性、生殖毒性、遗传毒性等一系列评估,明确安全剂量范围,才能获得进入人体试验的资格——这也是毒理学评估“源头排雷”的核心价值。
应用二:生产过程控险,守住杂质与工艺安全关
药品生产过程中,难免会产生杂质(如工艺杂质、降解产物)、残留(如溶剂残留、重金属残留),这些杂质哪怕含量极低,也可能对人体造成长期伤害。毒理学评估的核心作用,就是为这些杂质设定“安全限度”,确保生产过程的质量可控。经典案例就是华海药业缬沙坦NDMA事件(2018年)。
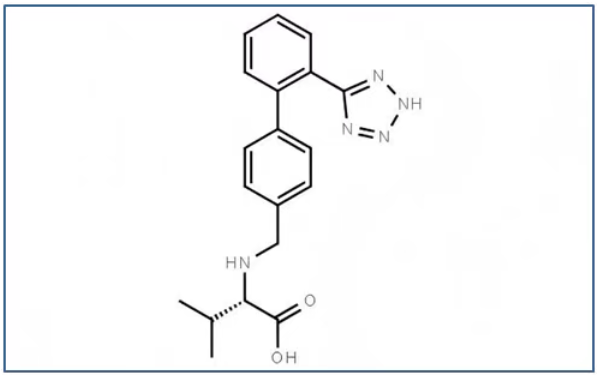
图3 缬沙坦的分子结构式
缬沙坦是常用的降压药,华海药业在生产缬沙坦原料药时,因工艺参数调整,产生了一种具有遗传毒性的杂质——N-亚硝基二甲胺(NDMA)。NDMA是2A类致癌物质(WHO/IARC),具基因毒性,长期摄入会增加患癌风险,但由于初期未对工艺变更后的杂质进行充分的毒理学评估,导致含有NDMA的缬沙坦原料药流入全球市场,引发大规模药品召回。
这一事件后,全球监管机构进一步强化了“杂质毒理学评估”的要求,依据毒理学评估数据,为NDMA等遗传毒性杂质设定了严格的安全限度(如每日允许暴露量PDE),同时要求企业在工艺变更后,必须重新开展杂质的毒理学评估,确保生产过程的每一个环节,都符合安全标准。
表1 N-亚硝基二甲胺(NDMA)的限量标准
除此之外,毒理学评估还能为药品辅料的选择提供依据——1937年美国磺胺酏剂事件,就是企业为降低成本,用工业溶剂二甘醇代替乙醇作为辅料,且未对二甘醇进行毒理学评估,最终导致107人死亡。这一事件推动了辅料毒理学评估的规范化,如今所有药品辅料,都必须通过毒理学评估,证明其在使用剂量下安全无毒,才能用于药品生产。
应用三:上市后护航,动态监控安全风险
药品上市后,毒理学评估依然发挥着重要作用——一方面,监测药品在长期使用中的慢性毒性、蓄积毒性;另一方面,针对上市后发现的新安全隐患,通过毒理学评估优化用药规范,降低风险。
还是以沙利度胺为例,其撤市后,科研人员通过进一步毒理学研究发现,沙利度胺的致畸性存在明显的“敏感期”:孕妇怀孕后第34~50天服用,最易导致胎儿畸形,且其致畸性与药物的手性结构相关(S型异构体致畸,R型异构体有镇静作用)。
基于这些毒理学研究数据,沙利度胺在后续被重新研发,用于治疗麻风结节性红斑、多发性骨髓瘤等疾病。但上市后,通过毒理学评估明确的风险,监管部门制定了严格的使用规范(如S.T.E.P.S.安全计划):仅允许注册机构销售,女性患者用药前需进行怀孕测试,用药期间及停药后4周需严格避孕,从源头规避致畸风险——这就是上市后毒理学评估“动态控险”的体现。
此外,上市后药品的剂量调整、特殊人群(老人、儿童、孕妇)用药指导,也都依赖毒理学评估数据。比如儿童用药的剂量,需通过动物毒理学试验,结合儿童的生理特点,推导安全剂量,避免因剂量过高导致毒性反应。
应用四:应急处置破局,快速定位药害事件根源
当药品出现安全隐患(如不良反应暴发)时,毒理学评估是快速定位根源、制定处置方案的核心手段。通过毒理学试验,可明确药品及其杂质的毒性作用机制、靶器官,判断不良反应与药品的关联度,为召回、停产、用药警示提供科学依据。
比如某款抗生素上市后,部分患者出现严重肝损伤,通过毒理学评估发现,是药品中的一种降解产物具有肝毒性,且生产过程中温度控制不当会导致该降解产物含量超标。基于这一结论,企业调整生产工艺,召回不合格产品,同时在说明书中增加肝损伤警示——毒理学评估快速破解了安全危机,减少了伤害范围。
天鉴检测:以专业毒理能力,做药品安全权威守门人
作为国内领先的第三方检测与技术服务机构,天鉴团队深耕药品质量和安全领域,团队成员由来自药学、生物学、毒理、分析化学及质量管理等不同领域的专家组成,具备多年药品毒理学评估与安全性研究经验,熟练开展基因毒性杂质评估、致癌性风险分析、急性 / 亚慢性毒性评价等工作,深度参与过亚硝胺类杂质、元素杂质等重点毒性物质的风险控制方案设计,熟悉国内外药监机构(NMPA、FDA、EMA)相关技术要求,能够为药品研发、申报及质量控制提供完整、合规的毒理学支持。天鉴检测期待用毒理专业的能力与您一起做药品安全的“守门员”。
[声明]本网转载网络媒体稿件是为了传播更多的信息,此类稿件不代表本网观点,本网不承担此类稿件侵权行为的连带责任。故此,如果您发现本网站的内容侵犯了您的版权,请您的相关内容发至此邮箱【service@skyte.com.cn】,我们在确认后,会立即删除,保证您的版权。
最新发布
- 药品安全“隐形守门人”|毒理学评估:从源头到终端,守护每一粒药的安全底
- 喜报!天鉴检测职业卫生资质延续获批,守护职业健康再启新程
- 大沙南路南侧16.2349亩储备用地土壤污染状况调查报告(第一阶段)
- 海口综合保税区(老城园区)保障性租赁住房及配套设施项目
- JP25120998深圳市敏特达电子有限公司网上公开信息表
- JP26120028_裕富宝厨具设备(深圳)有限公司网上公开信息表
- JP26120028_裕富宝厨具设备(深圳)有限公司网上公开信息表
- JP26120005_深圳市汉华光电子有限公司 网上公开信息表
- JP25121026_天品纽扣制品(深圳)有限公司工作场所职业病危害因素检测报告网上公开信息表
- JP25120938迈特通信设备(苏州)有限公司深圳分公司网上公开信息表
相关资讯
- JP25120041 佛山市高明毅力温控器有限公司 职业病危害因素定期报告网上公开信息表
- JP23120470 广东蓝特精密机械有限公司职业病危害因素定期报告网上公开信息表
- 【产品检测】天鉴检测客户满意度调查表
- 喜报!天鉴检测职业卫生资质延续获批,守护职业健康再启新程
- 策马奔腾 共赴新程——天鉴检测2025年优秀表彰暨2026年工作启动会成功举办
- 我司参加上海市药品检验研究院组织的能力验证项目,结果为“满意”!
- 我司参加“深圳市生态环境监测站”组织的能力验证项目,结果为“满意”!
- 天鉴检测完成广东省2025年度肥料质量抽查抽检!覆盖八市抽检75批次
- 我司参加“广东省职业病防治院”组织的能力验证项目,结果为“合格”!
- 我司参加“生态环境部环境发展中心”组织的能力验证项目,结果为“满意”!


